셀트리온, 램시마SC 임상 3상 결과 발표… “기존 제형과 효능 동일하고 치료 편의 개선”
- 동아경제
-
입력 2020년 10월 27일 11시 31분
공유하기
글자크기 설정
램시마SC RA 환자 대상 임상 3상 결과 공개
구연 및 포스터 발표 4건 선정
글로벌 10조 원 규모 시장 창출 기대

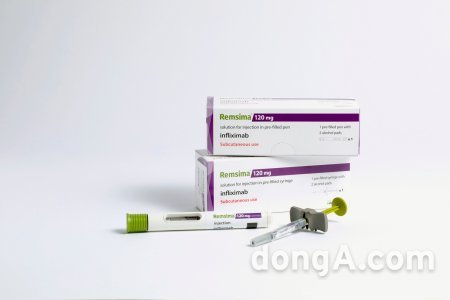
셀트리온은 최근 온라인으로 개최된 ‘2020 아시아태평양 류마티스학회(APLAR, Asia Pacific League of Associations for Rheumatology)’를 통해 세계 최초 인플릭시맙 피하주사 제형 자가면역질환 치료제 ‘램시마SC’의 류마티스관절염(RA, Rheumatoid Arthritis) 적응증 임상 3상 결과를 발표했다고 27일 밝혔다.
APLAR는 매년 4000명 넘는 아시아태평양지역 RA 전문가가 참석하는 아·태지역 최대 규모 학회다. 올해는 코로나19 영향으로 온라인으로 열렸다.
이번 학회에서 셀트리온은 1년간 램시마SC 면역원성에 대한 3상 데이터 영향 평가 결과를 구연 발표했다. 연구는 류마티스관절염 환자 343명을 대상으로 30주까지 램시마 정맥주사(Ⅳ) 데형과 피하주사(SC) 제형을 각각 투여한 후 54주까지 격주로 램시마SC를 전체 투여하는 방식으로 진행됐다. 그 결과 유의미한 항체 반응(ADA, Anti-drug Antibody) 지표를 확인했고 제형에 따른 면역원성 차이가 없다는 것을 입증했다.
이상준 셀트리온 임상개발본부 수석부사장은 “의료계 니즈에 따라 개발된 램시마SC의 안전성과 효과가 임상 결과를 통해 입증된 만큼 자가면역질환 치료제 시장의 글로벌 블록버스터 의약품으로 육성할 수 있도록 지속 노력할 것”이라고 전했다.
램시마SC는 지난해 11월 RA 적응증으로 유럽의약품청(EMA) 승인을 받고 올해 초 유럽시장에 본격 출시됐다. 지난 7월 EMA로부터 염증성 장질환(IBD, Inflammatory Bowel Disease) 적응증을 추가로 승인 받았다. 기존 램시마의 모든 성인 적응증을 획득한 것이다. 셀트리온은 기존 램시마 정맥주사 제형의 빠른 투약 효과에 피하주사 제형의 치료 편의성을 결함시킨 램시마SC가 전 세계 55조 원 규모 TNF-α(종양괴사인자) 억제제 시장을 효과적으로 공략할 수 있을 것으로 보고 있다. 약 10조 원 규모 신규 시장 창출을 기대하고 있다.
동아닷컴 김민범 기자 mbkim@donga.com
트렌드뉴스
-
1
“개인회생 신청했습니다” 집주인 통보받은 세입자가 할 일
-
2
다카이치가 10년 넘게 앓은 ‘이 병’…韓 인구의 1% 겪어
-
3
연금 개시 가능해지면 年 1만 원은 꼭 인출하세요[은퇴 레시피]
-
4
취권하는 중국 로봇, ‘쇼’인 줄 알았더니 ‘데이터 스펀지’였다?[딥다이브]
-
5
야상 입은 이정현 “당보다 지지율 낮은데 또 나오려 해”…판갈이 공천 예고
-
6
트럼프, 분노의 질주…“글로벌 관세 10%→15%로 인상”
-
7
트럼프, 세계에 10% 관세 때렸다…24일 발효, 승용차는 제외
-
8
블랙핑크, ‘레드 다이아’ 버튼 받았다…세계 아티스트 최초
-
9
“넌 이미 엄마 인생의 금메달”…최민정, 母손편지 품고 뛰었다
-
10
전원주 “벌써 자식들이 재산 노려…인감도장 달래”
-
1
국힘 전현직 당협위원장 20여명, ‘절윤 거부’ 장동혁에 사퇴 촉구
-
2
목줄 없이 산책하던 반려견 달려들어 50대 사망…견주 실형
-
3
김인호 산림청장 분당서 음주운전 사고…李, 직권면직
-
4
與 “尹 교도소 담장 못나오게” 내란범 사면금지법 처리 속도전
-
5
국토장관 “60억 아파트 50억으로…주택시장, 이성 되찾아”
-
6
張, 절윤 대신 ‘尹 어게인’ 유튜버와 한배… TK-PK의원도 “충격”
-
7
전원주 “벌써 자식들이 재산 노려…인감도장 달래”
-
8
‘면직’ 산림청장, 술 취해 무법질주…보행자 칠뻔, 車 2대 ‘쾅’
-
9
국힘 새 당명 ‘미래연대’-‘미래를 여는 공화당’ 압축
-
10
[사설]범보수마저 경악하게 한 張… ‘尹 절연’ 아닌 ‘당 절단’ 노리나
트렌드뉴스
-
1
“개인회생 신청했습니다” 집주인 통보받은 세입자가 할 일
-
2
다카이치가 10년 넘게 앓은 ‘이 병’…韓 인구의 1% 겪어
-
3
연금 개시 가능해지면 年 1만 원은 꼭 인출하세요[은퇴 레시피]
-
4
취권하는 중국 로봇, ‘쇼’인 줄 알았더니 ‘데이터 스펀지’였다?[딥다이브]
-
5
야상 입은 이정현 “당보다 지지율 낮은데 또 나오려 해”…판갈이 공천 예고
-
6
트럼프, 분노의 질주…“글로벌 관세 10%→15%로 인상”
-
7
트럼프, 세계에 10% 관세 때렸다…24일 발효, 승용차는 제외
-
8
블랙핑크, ‘레드 다이아’ 버튼 받았다…세계 아티스트 최초
-
9
“넌 이미 엄마 인생의 금메달”…최민정, 母손편지 품고 뛰었다
-
10
전원주 “벌써 자식들이 재산 노려…인감도장 달래”
-
1
국힘 전현직 당협위원장 20여명, ‘절윤 거부’ 장동혁에 사퇴 촉구
-
2
목줄 없이 산책하던 반려견 달려들어 50대 사망…견주 실형
-
3
김인호 산림청장 분당서 음주운전 사고…李, 직권면직
-
4
與 “尹 교도소 담장 못나오게” 내란범 사면금지법 처리 속도전
-
5
국토장관 “60억 아파트 50억으로…주택시장, 이성 되찾아”
-
6
張, 절윤 대신 ‘尹 어게인’ 유튜버와 한배… TK-PK의원도 “충격”
-
7
전원주 “벌써 자식들이 재산 노려…인감도장 달래”
-
8
‘면직’ 산림청장, 술 취해 무법질주…보행자 칠뻔, 車 2대 ‘쾅’
-
9
국힘 새 당명 ‘미래연대’-‘미래를 여는 공화당’ 압축
-
10
[사설]범보수마저 경악하게 한 張… ‘尹 절연’ 아닌 ‘당 절단’ 노리나
-
- 좋아요
- 0개
-
- 슬퍼요
- 0개
-
- 화나요
- 0개



댓글 0