공유하기
식약처, 코로나 항체치료제 ‘렉키로나’ 정식 허가…“치료 환자군 확대”
- 뉴시스
-
입력 2021년 9월 17일 17시 14분
글자크기 설정
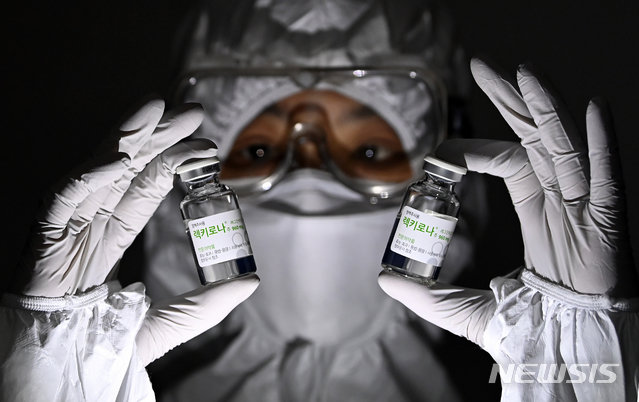
식품의약품안전처는 셀트리온의 코로나19 항체치료제 ‘렉키로나주’(성분명 레그단비맙)를 정식으로 품목허가 했다고 17일 밝혔다.
앞서 렉키로나는 지난 2월 식약처로부터 임상 3상 수행을 조건으로 조건부 허가받은 바 있다.
이번 정식 허가는 셀트리온이 글로벌 3상을 종료해 그 결과를 보고한 것에 따른 결정이다. 식약처는 기존에 ‘고위험군 경증에서 중등증 코로나19 환자의 임상증상 개선’에 사용하도록 허가한 것을 이번에 ‘고위험군 경증 및 모든 중등증 코로나19 환자의 치료’로 변경했다.
투여 시간도 90분간 정맥투여에서 60분으로 단축됐다.
렉키로나는 13개국에서 진행된 1315명 대상 3상 결과 안정성과 유효성을 확보했다. 렉키로나를 투여한 고위험군 환자군에선 중증환자 발생률이 위약군 대비 72%, 전체 환자에선 70% 감소했다.
식약처는 “전문가 자문 및 중앙약사심의위원회 자문 결과 정식 허가 전환 및 고위험군 범위 확대, 적용 대상을 고위험군 경증과 모든 중등증 성인 환자로 하는 것이 바람직하다고 의견을 모았다”고 설명했다.
다만, 고위험이 아닌 경증의 경우 중증 이환 빈도가 낮아 효과성에 대한 확증이 부족하므로 사용 범위에 포함시키지 않았다. 12세 이상 소아도 임상시험 대상에 포함되지 않아 사용 범위에 포함하지 않는 것이 타당하다는 의견을 제시했다.
셀트리온 관계자는 “식약처의 정식 품목허가는 렉키로나의 코로나19 바이러스 치료 효과에 대한 전문가들의 객관적이고 과학적인 판단에 의해 이뤄진 결과다”며 “다양한 변이 바이러스에도 대응할 수 있도록 노력을 기울이겠다”고 말했다.
[서울=뉴시스]
코로나 재확산 >
구독
트렌드뉴스
-
1
“청산 중”이라던 김용남 차명 대부업체, 실제론 등록 갱신 논란
-
2
“AI가 대체 못하는 ‘이것’ 갖춰야”…MIT 최순원 교수가 본 미래 인재상은?
-
3
선거벽보서 김태흠 뺀 충남선관위…“작업 실수, 후보자에 사과”
-
4
북한군 간호사에서 세계 누비는 사업가 되기까지[주성하의 북에서 온 이웃]
-
5
文 정부 때도 추진했던 ‘일베’ 폐쇄…이번엔 가능할까
-
6
양지호, 한국오픈 새역사…“힘들어 쉴까 했는데, 대리기사 불러 준 아내 덕”
-
7
정용진, 26일 대국민 사과…스벅 진상조사 결과도 발표
-
8
이회창 전 총재 부인 한인옥 여사 별세…향년 88세
-
9
“美-이란, MOU 체결시 호르무즈 통행량 전쟁 전 수준 회복”
-
10
“합의안 반대” DX조합원 1만명 늘자… 초기업노조 “투표 제외”
-
1
李 “일베 등 혐오 조장 사이트 폐쇄-징벌 배상 검토 지시할 것”
-
2
선거벽보서 김태흠 뺀 충남선관위…“작업 실수, 후보자에 사과”
-
3
정용진, 26일 대국민 사과…스벅 진상조사 결과도 발표
-
4
“북측” 지칭에 발끈한 北축구단, 기자회견장 박차고 나갔다
-
5
보령 간 장동혁 “내 얼굴 보고 김태흠 한번 더 뽑아달라”
-
6
선거판 돌아온 박근혜…대구 상인들 “사랑합니다” 손하트
-
7
“스벅 인증샷 올려라”…이수정, 국힘 유세서 ‘스벅 이용’ 독려
-
8
李, 스벅 또 직격 “일베도 아니고…세월호 추모일에 사이렌 이벤트”
-
9
“이준석 액을 매불쇼로 막아” 공연곡 논란에…5·18 행사위 ‘사과’
-
10
李 “盧 못다 이룬 개혁 추진…결코 물러서지 않겠다”
트렌드뉴스
-
1
“청산 중”이라던 김용남 차명 대부업체, 실제론 등록 갱신 논란
-
2
“AI가 대체 못하는 ‘이것’ 갖춰야”…MIT 최순원 교수가 본 미래 인재상은?
-
3
선거벽보서 김태흠 뺀 충남선관위…“작업 실수, 후보자에 사과”
-
4
북한군 간호사에서 세계 누비는 사업가 되기까지[주성하의 북에서 온 이웃]
-
5
文 정부 때도 추진했던 ‘일베’ 폐쇄…이번엔 가능할까
-
6
양지호, 한국오픈 새역사…“힘들어 쉴까 했는데, 대리기사 불러 준 아내 덕”
-
7
정용진, 26일 대국민 사과…스벅 진상조사 결과도 발표
-
8
이회창 전 총재 부인 한인옥 여사 별세…향년 88세
-
9
“美-이란, MOU 체결시 호르무즈 통행량 전쟁 전 수준 회복”
-
10
“합의안 반대” DX조합원 1만명 늘자… 초기업노조 “투표 제외”
-
1
李 “일베 등 혐오 조장 사이트 폐쇄-징벌 배상 검토 지시할 것”
-
2
선거벽보서 김태흠 뺀 충남선관위…“작업 실수, 후보자에 사과”
-
3
정용진, 26일 대국민 사과…스벅 진상조사 결과도 발표
-
4
“북측” 지칭에 발끈한 北축구단, 기자회견장 박차고 나갔다
-
5
보령 간 장동혁 “내 얼굴 보고 김태흠 한번 더 뽑아달라”
-
6
선거판 돌아온 박근혜…대구 상인들 “사랑합니다” 손하트
-
7
“스벅 인증샷 올려라”…이수정, 국힘 유세서 ‘스벅 이용’ 독려
-
8
李, 스벅 또 직격 “일베도 아니고…세월호 추모일에 사이렌 이벤트”
-
9
“이준석 액을 매불쇼로 막아” 공연곡 논란에…5·18 행사위 ‘사과’
-
10
李 “盧 못다 이룬 개혁 추진…결코 물러서지 않겠다”
-
- 좋아요
- 0개
-
- 슬퍼요
- 0개
-
- 화나요
- 0개




댓글 0