SK바이오팜 뇌전증 치료 신약 ‘세노바메이트’, 이스라엘 시판허가 획득
- 동아경제
-
입력 2023년 5월 3일 19시 07분
공유하기
글자크기 설정
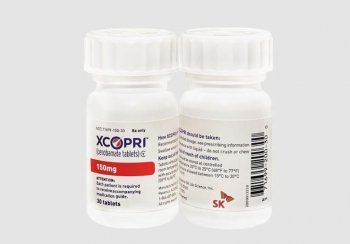
SK바이오팜은 뇌전증 치료 혁신신약 ‘세노바메이트(현지명 엑스코프리, XCOPRI)’가 최근 이스라엘 보건부(Ministry of Health)로부터 시판허가를 승인받았다고 3일 밝혔다. SK바이오팜 현지 파트너업체 덱셀파마(Dexcel)이 해당 허가 절차를 담당했다.
세노바메이트 12.5mg과 25mg, 50mg, 100mg, 150mg, 200mg 등 총 6개 용량이 이번 허가에 포함됐다. 세노베메이트는 SK바이오팜 주력 품목으로 성인 환자 부분발작 증상을 치료하는 뇌전증 치료제다. 미국 식품의약국(FDA) 승인을 받아 현지 시장에서 판매가 확대되는 추세다. 전압개폐성 나트륨 전류 차단을 통해 신경세포의 반복적인 발화를 감소시켜 성인 환자의 발작을 완화시키는 것으로 알려졌다.
SK바이오팜은 현재 전신 강직-간대 발작 포함 적응증을 확대하고 투약 가능 연령층을 넓히기 위해 국내외에서 다국가 임상을 진행하고 있다. 국내에서는 부분발작 증상이 있는 성인 환자를 대상으로 임상 3상이 이뤄지고 있다.
© dongA.com All rights reserved. 무단 전재, 재배포 및 AI학습 이용 금지
트렌드뉴스
-
1
오늘 세기의 종전 담판… 호르무즈 날 선 신경전
-
2
판교 한 채가 공주에선 네 채… 빚 갚던 부부, 이젠 저축[은퇴 레시피]
-
3
실종 70대 선장 찾은 잠수사, 하재숙 남편이었다
-
4
SK하이닉스 내년 1인당 성과급 13억? 로또급 전망 나왔다
-
5
경찰, 전한길 구속영장 신청…李대통령·이준석 명예훼손 혐의
-
6
“달리거나 계단 오를 땐 가슴통증, 쉬면 멀쩡… 혹시 협심증?”[베스트 닥터의 베스트 건강법]
-
7
[단독]“강남 재건축 적극 지원… 오세훈보다 더 빠르고 안전하게 할것”
-
8
“5일 굶었다” 편지 남기고 무인가게 음식 가져간 일용직…점주 반응은?
-
9
‘전쟁 추경’ 26.2조 통과… 소득하위 70% 지원금 유지
-
10
음료 가져간 알바에 합의금 550만원…더본코리아, 점주 영업정지
-
1
李 “정규직 선발되면 좋은 대우 받아야 한다?…상당히 큰 왜곡”
-
2
[단독]“사장이 성폭행” 경찰 신고한 20대 주점 알바, 무혐의 처리에 ‘이의 신청서’ 쓰고 목숨 끊어
-
3
與 ‘추미애 후폭풍’ 서둘러 봉합… 국힘선 ‘경기지사 기권패’ 우려
-
4
합수본 “전재수 통일교 금품의혹 무혐의”…사법리스크 풀어줬다
-
5
트럼프 “이란, 호르무즈 통행료 부과 당장 중단하라”
-
6
“저는 김창민 감독 살해범입니다” 유튜브 출연해 사과한 가해자
-
7
민주 48%, 국힘 20%, 무당층 25%…李 지지율은 67%
-
8
한동훈 “나는 읽기 쉬운 마음, 부산에 깊은 애정”…북구갑 출마 시사
-
9
“낮은 IQ” “미치광이”…‘휴전’ 트럼프, 이란전 비판 MAGA와 ‘전쟁’
-
10
한동훈 ‘부산 북갑 출마’ 가시권…국힘 후보 내야하나 논란 확산
트렌드뉴스
-
1
오늘 세기의 종전 담판… 호르무즈 날 선 신경전
-
2
판교 한 채가 공주에선 네 채… 빚 갚던 부부, 이젠 저축[은퇴 레시피]
-
3
실종 70대 선장 찾은 잠수사, 하재숙 남편이었다
-
4
SK하이닉스 내년 1인당 성과급 13억? 로또급 전망 나왔다
-
5
경찰, 전한길 구속영장 신청…李대통령·이준석 명예훼손 혐의
-
6
“달리거나 계단 오를 땐 가슴통증, 쉬면 멀쩡… 혹시 협심증?”[베스트 닥터의 베스트 건강법]
-
7
[단독]“강남 재건축 적극 지원… 오세훈보다 더 빠르고 안전하게 할것”
-
8
“5일 굶었다” 편지 남기고 무인가게 음식 가져간 일용직…점주 반응은?
-
9
‘전쟁 추경’ 26.2조 통과… 소득하위 70% 지원금 유지
-
10
음료 가져간 알바에 합의금 550만원…더본코리아, 점주 영업정지
-
1
李 “정규직 선발되면 좋은 대우 받아야 한다?…상당히 큰 왜곡”
-
2
[단독]“사장이 성폭행” 경찰 신고한 20대 주점 알바, 무혐의 처리에 ‘이의 신청서’ 쓰고 목숨 끊어
-
3
與 ‘추미애 후폭풍’ 서둘러 봉합… 국힘선 ‘경기지사 기권패’ 우려
-
4
합수본 “전재수 통일교 금품의혹 무혐의”…사법리스크 풀어줬다
-
5
트럼프 “이란, 호르무즈 통행료 부과 당장 중단하라”
-
6
“저는 김창민 감독 살해범입니다” 유튜브 출연해 사과한 가해자
-
7
민주 48%, 국힘 20%, 무당층 25%…李 지지율은 67%
-
8
한동훈 “나는 읽기 쉬운 마음, 부산에 깊은 애정”…북구갑 출마 시사
-
9
“낮은 IQ” “미치광이”…‘휴전’ 트럼프, 이란전 비판 MAGA와 ‘전쟁’
-
10
한동훈 ‘부산 북갑 출마’ 가시권…국힘 후보 내야하나 논란 확산
-
- 좋아요
- 0개
-
- 슬퍼요
- 0개
-
- 화나요
- 0개



댓글 0