구충제 성분 코로나19 치료제 임상 돌입… 대웅제약, 인도서 ‘니클로사마이드’ 임상 1상 승인
- 동아경제
-
입력 2020년 8월 11일 15시 03분
공유하기
글자크기 설정
인도 이어 미국·유럽 등 선진국 허가 추진
인도, 코로나19 확산 글로벌 최고 수준
하반기 내 임상 1상 완료 목표
‘니클로사마이드·카모스타트·줄기세포’ 치료제 개발 중
“무증상부터 중증까지 아우르는 치료제 라인업 갖출 것”
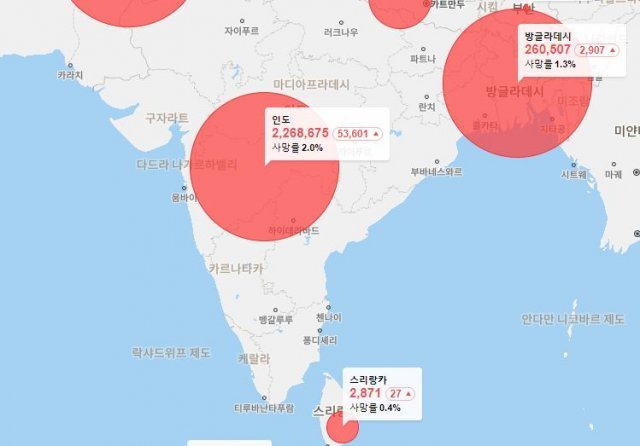
대웅제약이 인도에서 구충제 성분 신종 코로나바이러스감염증(코로나19) 치료제 임상 1상 승인을 받았다.
질병관리본부에 따르면 인도는 코로나19 확진자가 226만8675명으로 미국(약 507만 명)과 브라질(약 305만 명)에 이어 세 번째로 확진자 규모가 큰 국가다. 8월 11일 기준 하루 동안 확인된 확진 환자 수는 5만3601명이다. 확진자 수가 많은 미국(4만8816명)과 브라질(2만2048명)보다 확산세가 두드러진다.
대웅제약은 11일 인도 중앙의약품표준관리국(CDSCO)으로부터 코로나19 치료제 ‘DWRX2003(성분명 니클로사마이드)’ 임상 1상 시험을 승인 받았다고 밝혔다. 글로벌 코로나19 치료제 개발 가속화를 위해 후보물질 니클로사마이드 임상시험을 국내는 물론 해외까지 확대 추진한다는 방침이다. 국내에서도 현재 임상 1상 추진을 위한 신청 접수가 들어간 상태다.

이번 임상 1상은 건강한 피험자 약 30여명을 대상으로 인도 현지에서 진행된다. 8월 중 피험자에게 첫 투여를 시작해 하반기 내 1상을 완료한다는 계획이다. 이후 경증환자와 중등증환자를 대상으로 한 임상 2·3상을 올해 인도에서 개시하고 결과가 확보되는 대로 현지 허가를 신청할 예정이다.
대웅제약은 니클로사마이드 임상 가속화와 신속한 현지 공급을 위해 인도 3위 제약사 ‘맨카인드파마(Mankind Pharma)’와 라이선스 및 공동개발 협약을 체결했다. 임상 1상 시험은 대웅제약 인도법인이 메인 스폰서, 맨카인드파마가 공동 스폰서로 참여해 이뤄진다. 맨카인드파마가 남은 2상과 3상 임상도 담당하게 된다. 이번 인도 임상결과는 미국과 유럽 등 선진국 허가 제출을 위한 자료로도 활용한다는 계획이다.
동아닷컴 김민범 기자 mbkim@donga.com
트렌드뉴스
-
1
“하메네이 사망” 트럼프 공식 발표…“일주일간 폭격할 것”
-
2
집무실 ‘가루’ 된 하메네이, 생사 불확실…권력 계승자 4명 정해놔
-
3
[단독]폴란드, 韓 해군 최초 잠수함 ‘장보고함’ 무상 양도 안받기로
-
4
中 “美의 이란 공습 즉각 중단해야…이란 주권과 영토 보전 존중”
-
5
‘부화방탕 대명사’ 북한 2인자 최룡해의 퇴장 [주성하의 ‘北토크’]
-
6
지지율 하락을 전쟁으로 만회?…트럼프 ‘이란 공격’ 진짜 이유는
-
7
“내 항공권 어쩌나” 도하 영공 전면 폐쇄…중동 하늘길 막혔다
-
8
‘총 쏘는 13세 김주애’ 단독샷 이례적 공개…또 가죽점퍼
-
9
상호관세 막히자 ‘301조’ 꺼낸 트럼프…‘쿠팡 사태’ 3월 7일 조사 분수령
-
10
공습 시작에 테헤란 직장인들, 울며 자녀 학교로 뛰어가…검은 토요일
-
1
장동혁, 이준석-전한길 토론 보더니 “부정선거 막을 시스템 필요”
-
2
‘대법관 증원법’ 가결…李대통령이 26명 중 22명 임명한다
-
3
국민 64%가 “내란” 이라는데… 당심만 보며 민심 등지는 국힘
-
4
대구 간 한동훈 “죽이되든 밥이되든 나설것”
-
5
송광사 찾은 李대통령 내외…“고요함 속 다시 힘 얻어”
-
6
큰 거 온다더니 ‘틱톡커 이재명’…“팔로우 좋아요 아시죠?”
-
7
[책의 향기]무기 팔고자 위협을 제조하는 美 군산복합체
-
8
‘지지율 바닥’ 쇼크에도… 민심과 따로 가는 국힘
-
9
이란, 중동 美기지 4곳 ‘조준 공격’…“미군 4만명 이란 사정권”
-
10
“하메네이 사망” 트럼프 공식 발표…“일주일간 폭격할 것”
트렌드뉴스
-
1
“하메네이 사망” 트럼프 공식 발표…“일주일간 폭격할 것”
-
2
집무실 ‘가루’ 된 하메네이, 생사 불확실…권력 계승자 4명 정해놔
-
3
[단독]폴란드, 韓 해군 최초 잠수함 ‘장보고함’ 무상 양도 안받기로
-
4
中 “美의 이란 공습 즉각 중단해야…이란 주권과 영토 보전 존중”
-
5
‘부화방탕 대명사’ 북한 2인자 최룡해의 퇴장 [주성하의 ‘北토크’]
-
6
지지율 하락을 전쟁으로 만회?…트럼프 ‘이란 공격’ 진짜 이유는
-
7
“내 항공권 어쩌나” 도하 영공 전면 폐쇄…중동 하늘길 막혔다
-
8
‘총 쏘는 13세 김주애’ 단독샷 이례적 공개…또 가죽점퍼
-
9
상호관세 막히자 ‘301조’ 꺼낸 트럼프…‘쿠팡 사태’ 3월 7일 조사 분수령
-
10
공습 시작에 테헤란 직장인들, 울며 자녀 학교로 뛰어가…검은 토요일
-
1
장동혁, 이준석-전한길 토론 보더니 “부정선거 막을 시스템 필요”
-
2
‘대법관 증원법’ 가결…李대통령이 26명 중 22명 임명한다
-
3
국민 64%가 “내란” 이라는데… 당심만 보며 민심 등지는 국힘
-
4
대구 간 한동훈 “죽이되든 밥이되든 나설것”
-
5
송광사 찾은 李대통령 내외…“고요함 속 다시 힘 얻어”
-
6
큰 거 온다더니 ‘틱톡커 이재명’…“팔로우 좋아요 아시죠?”
-
7
[책의 향기]무기 팔고자 위협을 제조하는 美 군산복합체
-
8
‘지지율 바닥’ 쇼크에도… 민심과 따로 가는 국힘
-
9
이란, 중동 美기지 4곳 ‘조준 공격’…“미군 4만명 이란 사정권”
-
10
“하메네이 사망” 트럼프 공식 발표…“일주일간 폭격할 것”
-
- 좋아요
- 0개
-
- 슬퍼요
- 0개
-
- 화나요
- 0개



댓글 0