美 FDA, 오는 5월 한미약품 ‘롤론티스’ 생산 시설 실사… “현지 공무원 여행 제한 완화”
- 동아경제
-
입력 2021년 3월 17일 17시 34분
공유하기
글자크기 설정
코로나19 영향으로 실사 일정 연기
‘롤론티스’ 미국 판매 허가 마지막 단계
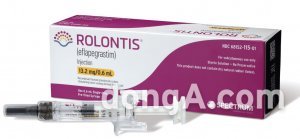
한미약품은 미국 식품의약국(FDA)으로부터 바이오신약 ‘롤론티스’ 원액을 생산하는 평택 바이오플랜트에 대한 ‘승인 전 실사(pre-approval inspection)’를 오는 5월 중 진행하겠다는 통보를 받았다고 17일 밝혔다. 해당 실사는 코로나19 팬데믹 영향으로 미국 공무원들의 여행이 제한되면서 잠정 연기된 상태였다.
롤론티스는 한미약품 독자 플랫폼 기술인 ‘랩스커버리’가 적용된 바이오의약품으로 항암화학요법을 받는 암 환자에서 발생하는 호중구감소증 치료 또는 예방 용도로 투여되는 약효 지속형 신약이다.
한미약품 파트너업체 스펙트럼 조 터전(Joe Turgeon) 사장은 “FDA의 롤론티스 제조시설 실사 일정이 확정된 것을 환영한다”며 “이번 FDA 실사는 롤론티스 미국 판매 허가를 위한 마지막 단계가 될 것”이라고 전했다.
동아닷컴 김민범 기자 mbkim@donga.com
트렌드뉴스
-
1
덴마크 언론 “폭력배 트럼프”… 英국민 67% “美에 보복관세 찬성”
-
2
부부 합쳐 6차례 암 극복…“내 몸의 작은 신호 잘 살피세요”
-
3
[이진영 칼럼]잘난 韓, 못난 尹, 이상한 張
-
4
“하루 3분이면 충분”…헬스장 안 가도 건강해지는 ‘틈새 운동’법
-
5
김정은, 공장 준공식서 부총리 전격 해임 “그모양 그꼴밖에 안돼”
-
6
결국 날아온 노란봉투…금속노조 “하청, 원청에 교섭 요구하라”
-
7
82세 장영자, 또 사기로 실형…1982년부터 여섯 번째
-
8
‘오들오들’ 북극한파에 치솟는 혈압…‘이것’ 꼭 실천해야
-
9
강선우 “원칙 지키며 살아”… 前보좌관 “강선우 1억 받아 전세금 보태” 진술
-
10
단순 잇몸 염증인 줄 알았는데…8주 지나도 안 낫는다면
-
1
李대통령 “제멋대로 무인기 침투, 北에 총 쏜 것과 똑같다”
-
2
李대통령 “생리대 고급화하며 바가지…기본 제품 무상공급 검토”
-
3
강선우, 의혹 22일만에 경찰 출석…“원칙 지키는 삶 살았다”
-
4
‘평양 무인기 침투’ 尹 계획 실행한 드론사령부 해체된다
-
5
정청래 “비법률가인 나도 법사위원장 했다”…검사 권한 고수 비판
-
6
李 가덕도 피습, 정부 공인 첫 테러 지정…“뿌리를 뽑아야”
-
7
[속보]李대통령 “무인기 침투, 北에 총 쏜 것과 똑같다”
-
8
홍준표 “과거 공천 헌금 15억 제의받아…김병기·강선우 뿐이겠나”
-
9
“장동혁 죽으면 좋고” 김형주 막말에…국힘 “생명 조롱”
-
10
의사 면허 취소된 50대, 분식집 운영하다 극단적 선택
트렌드뉴스
-
1
덴마크 언론 “폭력배 트럼프”… 英국민 67% “美에 보복관세 찬성”
-
2
부부 합쳐 6차례 암 극복…“내 몸의 작은 신호 잘 살피세요”
-
3
[이진영 칼럼]잘난 韓, 못난 尹, 이상한 張
-
4
“하루 3분이면 충분”…헬스장 안 가도 건강해지는 ‘틈새 운동’법
-
5
김정은, 공장 준공식서 부총리 전격 해임 “그모양 그꼴밖에 안돼”
-
6
결국 날아온 노란봉투…금속노조 “하청, 원청에 교섭 요구하라”
-
7
82세 장영자, 또 사기로 실형…1982년부터 여섯 번째
-
8
‘오들오들’ 북극한파에 치솟는 혈압…‘이것’ 꼭 실천해야
-
9
강선우 “원칙 지키며 살아”… 前보좌관 “강선우 1억 받아 전세금 보태” 진술
-
10
단순 잇몸 염증인 줄 알았는데…8주 지나도 안 낫는다면
-
1
李대통령 “제멋대로 무인기 침투, 北에 총 쏜 것과 똑같다”
-
2
李대통령 “생리대 고급화하며 바가지…기본 제품 무상공급 검토”
-
3
강선우, 의혹 22일만에 경찰 출석…“원칙 지키는 삶 살았다”
-
4
‘평양 무인기 침투’ 尹 계획 실행한 드론사령부 해체된다
-
5
정청래 “비법률가인 나도 법사위원장 했다”…검사 권한 고수 비판
-
6
李 가덕도 피습, 정부 공인 첫 테러 지정…“뿌리를 뽑아야”
-
7
[속보]李대통령 “무인기 침투, 北에 총 쏜 것과 똑같다”
-
8
홍준표 “과거 공천 헌금 15억 제의받아…김병기·강선우 뿐이겠나”
-
9
“장동혁 죽으면 좋고” 김형주 막말에…국힘 “생명 조롱”
-
10
의사 면허 취소된 50대, 분식집 운영하다 극단적 선택
-
- 좋아요
- 0개
-
- 슬퍼요
- 0개
-
- 화나요
- 0개


댓글 0