美 임상 3상 마친 한미약품 ‘롤론티스’, 한국인 동일 효과 입증
- 동아경제
-
입력 2021년 4월 8일 18시 58분
공유하기
글자크기 설정
한미약품, 세계유방암학술대회서 임상 결과 2건 발표
인종간 약효 분석 결과 차이 無
롤론티스 지난달 국내 시판 허가
오는 5월 평택 바이오플랜트 美 FDA 실사
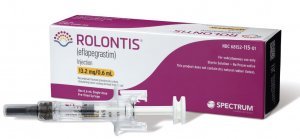
한미약품 호중구감소증치료제 ‘롤론티스’가 인종이 달라도 약효가 동일하다는 내용을 입증한 연구결과가 발표됐다.
한미약품은 미국 등 다국가 글로벌 임상 3상을 성공적으로 마친 롤론티스의 임상 분석 결과 2건을 세계유방암학술대회(GBCC)를 통해 발표했다고 8일 밝혔다.
올해 10회를 맞은 GBCC는 유방암을 다루는 30여개국 1300여명의 전문가들이 모여 최신 지견을 논의하는 국제학술대회다. 올해는 오는 10일까지 열린다.
한미약품은 초기 유방암 환자 총 643명을 무작위 배정해 항암화학요법 다음날 롤론티스 또는 활성대조약을 투여하는 방식으로 임상을 진행했다고 설명했다. 이를 토대로 한국인 소집단과 전체 모집단을 비교·분석했다. 분석 결과에 따르면 활성 대조약 대비 중증호중구감소증 발현기간(DSN, Duration of Severe Neutropenia)으로 확인된 롤론티스 비열등성은 한국인 소집단 분석에서 차이가 없는 것으로 나타났다. 다른 주요 2차 평가 변수인 호중구최저점 및 열성호중구감소증(Febrile Neutropeni) 발생률 또한 유의미한 차이가 없었고 전반적인 안전성 프로파일도 한국인과 전체 모집단이 유사한 것으로 나왔다. 해당 연구는 이번 학술대회 우수발표상 후보로도 지정됐다.
이와 함께 한미약품은 1상 임상 연구 2건을 바탕으로 한국인과 비한국인간 롤론티스 투여 용량별 약동학(PK) 및 약력학(PD)을 비교·분석한 연구결과를 포스터로 발표했다. 모든 인종에서 비슷한 약동학을 보였고 절대 호중구 수(ANC, Absolute Neutrophil Count)와 조혈모세포(CD34+ 세포) 수로 분석한 약력학도 인종간 차이가 없는 것으로 확인됐다고 전했다. 다수 글로벌 임상을 통해 증명한 롤론티스의 약동학 및 약력학적 특성이 한국인에게도 동일하게 적용될 수 있다는 것을 의미한다는 설명이다.
이 같은 결과를 토대로 지난 3월 국내 식품의약품안전처는 롤론티스를 한미약품의 첫 번째 바이오신약으로 시판 허가했다. 현재 한미약품은 롤론티스의 미국 시판 허가를 위해 오는 5월 실시되는 식품의약국(FDA)의 평택 바이오플랜트 실사를 준비하고 있다.
동아닷컴 김민범 기자 mbkim@donga.com
트렌드뉴스
-
1
단순 잇몸 염증인 줄 알았는데…8주 지나도 안 낫는다면
-
2
부부 합쳐 6차례 암 극복…“내 몸의 작은 신호 잘 살피세요”
-
3
[이진영 칼럼]잘난 韓, 못난 尹, 이상한 張
-
4
덴마크 언론 “폭력배 트럼프”… 英국민 67% “美에 보복관세 찬성”
-
5
“하루 3분이면 충분”…헬스장 안 가도 건강해지는 ‘틈새 운동’법
-
6
‘명청 프레임’ 불쾌한 李, 정청래 면전서 경고 메시지
-
7
21시간 조사 마친 강선우 ‘1억 전세금 사용설’ 묵묵부답
-
8
김정은, 공장 준공식서 부총리 전격 해임 “그모양 그꼴밖에 안돼”
-
9
결국 날아온 노란봉투…금속노조 “하청, 원청에 교섭 요구하라”
-
10
韓은 참여 선그었는데…트럼프 “알래스카 LNG, 韓日서 자금 확보”
-
1
李대통령 “제멋대로 무인기 침투, 北에 총 쏜 것과 똑같다”
-
2
李대통령 “생리대 고급화하며 바가지…기본 제품 무상공급 검토”
-
3
‘평양 무인기 침투’ 尹 계획 실행한 드론사령부 해체된다
-
4
강선우, 의혹 22일만에 경찰 출석…“원칙 지키는 삶 살았다”
-
5
[이진영 칼럼]잘난 韓, 못난 尹, 이상한 張
-
6
정청래 “비법률가인 나도 법사위원장 했다”…검사 권한 고수 비판
-
7
李 가덕도 피습, 정부 공인 첫 테러 지정…“뿌리를 뽑아야”
-
8
[속보]李대통령 “무인기 침투, 北에 총 쏜 것과 똑같다”
-
9
의사 면허 취소된 50대, 분식집 운영하다 극단적 선택
-
10
“장동혁 죽으면 좋고” 김형주 막말에…국힘 “생명 조롱”
트렌드뉴스
-
1
단순 잇몸 염증인 줄 알았는데…8주 지나도 안 낫는다면
-
2
부부 합쳐 6차례 암 극복…“내 몸의 작은 신호 잘 살피세요”
-
3
[이진영 칼럼]잘난 韓, 못난 尹, 이상한 張
-
4
덴마크 언론 “폭력배 트럼프”… 英국민 67% “美에 보복관세 찬성”
-
5
“하루 3분이면 충분”…헬스장 안 가도 건강해지는 ‘틈새 운동’법
-
6
‘명청 프레임’ 불쾌한 李, 정청래 면전서 경고 메시지
-
7
21시간 조사 마친 강선우 ‘1억 전세금 사용설’ 묵묵부답
-
8
김정은, 공장 준공식서 부총리 전격 해임 “그모양 그꼴밖에 안돼”
-
9
결국 날아온 노란봉투…금속노조 “하청, 원청에 교섭 요구하라”
-
10
韓은 참여 선그었는데…트럼프 “알래스카 LNG, 韓日서 자금 확보”
-
1
李대통령 “제멋대로 무인기 침투, 北에 총 쏜 것과 똑같다”
-
2
李대통령 “생리대 고급화하며 바가지…기본 제품 무상공급 검토”
-
3
‘평양 무인기 침투’ 尹 계획 실행한 드론사령부 해체된다
-
4
강선우, 의혹 22일만에 경찰 출석…“원칙 지키는 삶 살았다”
-
5
[이진영 칼럼]잘난 韓, 못난 尹, 이상한 張
-
6
정청래 “비법률가인 나도 법사위원장 했다”…검사 권한 고수 비판
-
7
李 가덕도 피습, 정부 공인 첫 테러 지정…“뿌리를 뽑아야”
-
8
[속보]李대통령 “무인기 침투, 北에 총 쏜 것과 똑같다”
-
9
의사 면허 취소된 50대, 분식집 운영하다 극단적 선택
-
10
“장동혁 죽으면 좋고” 김형주 막말에…국힘 “생명 조롱”
-
- 좋아요
- 0개
-
- 슬퍼요
- 0개
-
- 화나요
- 0개


댓글 0