공유하기
배아줄기세포 임상 첫 승인
- 동아일보
글자크기 설정
국생위, 차바이오社 ‘망막질환 치료제’ 찬성… 美이어 세계 두번째
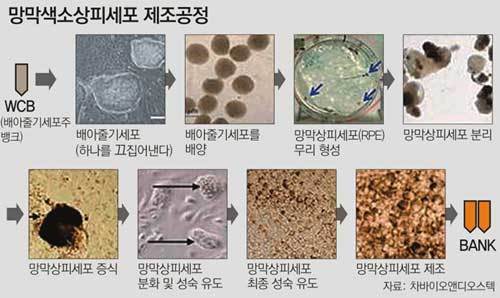
국내 처음으로 배아줄기세포를 이용한 임상시험의 길이 열렸다. 이 같은 임상시험 허가는 미국에 이어 세계 두 번째다.
국가생명윤리심의위원회(국생위)는 27일 바이오업체 차바이오앤디오스텍의 배아줄기세포로 망막질환 치료제를 만드는 임상시험이 생명윤리법을 어기지 않는다는 결론을 내렸다.
이에 따라 차바이오는 식품의약품안전청의 허가를 받는 대로 임상시험을 시작할 수 있다.
이번 임상이 승인되면 2005년 황우석 교수 논문조작 사태 이후 금기시돼 온 배아줄기세포를 이용한 세포치료제 개발이 본격화할 것으로 보인다. 국생위의 이번 결정도 난치성 치료제 개발을 더는 늦출 수 없다고 판단했기 때문으로 풀이된다. 노재경 국생위 위원장(연세대 의대 교수)은 “이번 임상은 배아줄기세포를 망막세포로 분화시킨 다음 사용한다. 이미 분화된 세포는 체내 이용이 금지된 배아줄기세포에 해당되지 않는다는 데 위원 전원이 찬성했다”고 말했다.
차바이오의 임상시험은 유전자 돌연변이로 청소년기에 빈번히 발생하는 스타가르트병 환자를 대상으로 진행된다. 이 병은 눈의 중심시력을 담당하는 황반에 이상이 생겨 발생하며 환자의 절반이 50세 이전에 실명하지만 적절한 치료법이 없다.
임상시험은 우선 환자 3명을 대상으로 18개월에 걸쳐 진행된다. 연구팀은 황반에 이상이 생겼을 때 제일 먼저 죽게 되는 망막색소상피세포(RPE)를 배아줄기세포로 만들어 환자에게 주입한다. 망막 기능을 되살려 시력을 회복시키는 것이다. 차바이오와 공동으로 연구를 해온 미국 바이오업체 ACT는 이미 지난해 11월 22일 미 식품의약국(FDA)의 허가를 받아 임상시험을 하고 있다.
한편 국생위는 인공수정 직후 냉동되지 않은 신선 배아세포를 분리 배양해 그 일부로 줄기세포를 만들려는 차병원의 연구 신청은 허용하지 않기로 했다. 할구를 증식한 배아세포를 생명의 일부로 간주했기 때문이다.
우경임 기자 woohaha@donga.com
이진한 기자·의사 likeday@donga.com
트렌드뉴스
-
1
“현주엽에게 학폭 당해” 인터넷에 올린 누리꾼 ‘무죄’ 확정
-
2
시속 153km 과속하다 중앙선 넘어 승객 숨지게 한 택시기사 ‘집유’
-
3
[오늘의 운세/5월 1일]
-
4
‘추다르크’ 추미애 vs ‘고졸신화’ 양향자…경기지사 ‘女대女’ 대결
-
5
임형주 150억 저택 공사비 미지급 논란…업체들 “3년째 못 받아”
-
6
삼전 노조에 뿔난 LG 노조 “비겁하고 경솔한 책임 전가…사과하라”
-
7
‘미스 춘향’에 우크라이나 유학생이?…경북대 대학원 재학 중
-
8
“3개월 통보했는데 왜 못 나가?”…전세 해지 뒤 막히는 ‘보증금’ [집과법]
-
9
엘베 버튼-버스 손잡이도 못 견디는 ‘오염 강박’…트럼프도 앓아
-
10
“여러분 때문에 국힘 안돼” “장동혁!”…박형준 개소식서 고성-항의
-
1
‘추다르크’ 추미애 vs ‘고졸신화’ 양향자…경기지사 ‘女대女’ 대결
-
2
美, 주독미군 5000명 철수 명령…나토 보복 현실화
-
3
삼바 노조 “영업익 20% 성과급” 전면파업… SK 하청도 배분 요구
-
4
삼전 노조에 뿔난 LG 노조 “비겁하고 경솔한 책임 전가…사과하라”
-
5
‘공소취소 특검법’ 앞에 똘똘 뭉치는 국힘 …“천인공노 할 짓”
-
6
李 “자기들만 살겠다고”…삼전 노조위원장 “우리 아니라 LG 얘기”
-
7
‘기관사 유니폼’ 다시 입은 고용장관…“노동의 눈 안 변해”
-
8
‘尹 어게인’ 재등판한 국힘… 대구달성 이진숙 - 하남갑 이용 공천
-
9
‘한동훈과 단일화 할거냐’ 국힘 면접질문에…韓 “나하고만 싸우려 해”
-
10
개소식 2곳 빼곤 연휴일정 없는 장동혁…국힘 “전략적 판단”
트렌드뉴스
-
1
“현주엽에게 학폭 당해” 인터넷에 올린 누리꾼 ‘무죄’ 확정
-
2
시속 153km 과속하다 중앙선 넘어 승객 숨지게 한 택시기사 ‘집유’
-
3
[오늘의 운세/5월 1일]
-
4
‘추다르크’ 추미애 vs ‘고졸신화’ 양향자…경기지사 ‘女대女’ 대결
-
5
임형주 150억 저택 공사비 미지급 논란…업체들 “3년째 못 받아”
-
6
삼전 노조에 뿔난 LG 노조 “비겁하고 경솔한 책임 전가…사과하라”
-
7
‘미스 춘향’에 우크라이나 유학생이?…경북대 대학원 재학 중
-
8
“3개월 통보했는데 왜 못 나가?”…전세 해지 뒤 막히는 ‘보증금’ [집과법]
-
9
엘베 버튼-버스 손잡이도 못 견디는 ‘오염 강박’…트럼프도 앓아
-
10
“여러분 때문에 국힘 안돼” “장동혁!”…박형준 개소식서 고성-항의
-
1
‘추다르크’ 추미애 vs ‘고졸신화’ 양향자…경기지사 ‘女대女’ 대결
-
2
美, 주독미군 5000명 철수 명령…나토 보복 현실화
-
3
삼바 노조 “영업익 20% 성과급” 전면파업… SK 하청도 배분 요구
-
4
삼전 노조에 뿔난 LG 노조 “비겁하고 경솔한 책임 전가…사과하라”
-
5
‘공소취소 특검법’ 앞에 똘똘 뭉치는 국힘 …“천인공노 할 짓”
-
6
李 “자기들만 살겠다고”…삼전 노조위원장 “우리 아니라 LG 얘기”
-
7
‘기관사 유니폼’ 다시 입은 고용장관…“노동의 눈 안 변해”
-
8
‘尹 어게인’ 재등판한 국힘… 대구달성 이진숙 - 하남갑 이용 공천
-
9
‘한동훈과 단일화 할거냐’ 국힘 면접질문에…韓 “나하고만 싸우려 해”
-
10
개소식 2곳 빼곤 연휴일정 없는 장동혁…국힘 “전략적 판단”
-
- 좋아요
- 0개
-
- 슬퍼요
- 0개
-
- 화나요
- 0개



댓글 0