공유하기
30억 DNA 중 돌연변이 1개만 골라 싹둑… 난치병 정복 첫발
- 동아일보
글자크기 설정
[토요기획]0.00000003%의 확률을 맞히는 유전자 가위 ‘크리스퍼’의 진화
가오쉐 미국 하버드대 화학 및 화학생물학과 연구원은 올해 내내 실험용 마우스(흰쥐)를 대상으로 한 실험에 열중해 있었다. 이 쥐의 이름은 베토벤. 천재 작곡가 이름과 같았다. 이 쥐에게 음악적 재능이 탁월해서 붙인 이름은 아니다. 사실 이름을 지은 것도 가오 박사가 아니다. 2002년, 처음 이 쥐를 탄생시키고 이름을 붙인 이스라엘 과학자들은 한 가지 특성이 보통 쥐와 다르다는 사실에 주목했다. 바로 귀가 들리지 않는다는 점이다.
18, 19세기에 활동한 작곡가 루트비히 판 베토벤은 20대 후반부터 귀가 잘 들리지 않다 44세에 거의 청력을 잃었다. 그가 청력을 잃은 이유는 밝혀지지 않았지만, 후천적인 병의 후유증 또는 유전적 요인 가운데 하나일 것이라고 추측된다.
과학자들은 둘 가운데 유전적 요인에 관심을 가졌다. 그리고 쥐를 이용한 실험 끝에 청력의 손상을 일으키는 유전자를 발견했다. Tmc1이라는 유전자가 정상과 다를 경우(이 유전자에 변이가 있을 경우), 귀 안쪽의 달팽이관에 있는 청각 신호 생성 세포(유모세포)에 일종의 노폐물 단백질이 만들어져 쌓인다는 사실도 밝혀냈다. 노폐물이 쌓이면 유모세포가 죽으면서 청력이 서서히 약해지고, 10∼15년 뒤에는 완전히 청력을 잃게 된다. 우연의 일치인지 알 수 없지만 베토벤이 청력을 잃기까지 걸린 시간과 비슷하다.
하지만 문제가 있다. DNA는 그렇게 쉽게 떼어내거나 바꿀 수 있는 물질이 아니다. 일단 무척 작다. 흔히 이중나선으로 묘사되는 DNA 한 가닥의 굵기는 머리카락의 10만 분의 1 정도인 1nm(나노미터·1nm는 10억 분의 1m)로, 인간이 만든 어떤 도구도 이렇게 작은 DNA를 직접 찾아 끊을 수 없다. 또 DNA 자체가 생명의 정보를 간직하고 있는 일종의 데이터베이스이다 보니 무엇보다 변형에 극도로 저항하는 성질이 있었다. 철사처럼 튼튼하고 고무줄처럼 질긴 생체 고분자 물질이 바로 DNA다.

난치성 병을 직접 고친 이 사례는 크리스퍼 기술이 올해 주도하고 있는 혁신의 한 단면이다. 성공적인 질병 치료 사례가 늘어나고 있다. 올해 2월에는 김정훈 서울대 병원 교수 팀과 김진수 기초과학연구원(IBS) 유전체교정연구단장 팀이 크리스퍼를 캡슐로 감싸 눈에 넣어 노인성 황반변성을 치료하고 실명을 예방하는 데에 세계 최초로 성공했다. 노인성 황반변성은 혈관이 없어야 할 황반에 혈관이 자라면서 시야를 가려 실명을 유발하는 병으로, 전체 실명 원인의 5%를 차지한다.
두 번째 혁신은 크리스퍼 기술 자체의 진보다. 특히 정확도가 더욱 높아졌다. 크리스퍼는 크게 두 가지 구성 요소로 이뤄진 생체 분자 기계다. 원하는 DNA를 찾을 수 있게 정보를 담고 있는 부위가 한 부분이고, DNA를 실제로 잘라 내는 일종의 절단효소가 한 부분이다. 가장 널리 연구되고 쓰이고 있는 크리스퍼는 절단효소로 ‘캐스9’를 쓰는 크리스퍼-캐스9이다.
2015년, 장펑 미국 매사추세츠공대(MIT) 교수팀은 캐스9보다 정확성이 높은 Cpf1이라는 효소를 이용하는 새로운 유전자 가위 ‘크리스퍼-Cpf1’을 개발했다. 김진수 단장 팀은 작년 6월 신형 크리스퍼-Cpf1의 정확성을 기존 크리스퍼-캐스9와 비교하는 연구를 했다. 그 결과 새로운 크리스퍼가 DNA 30억 쌍 중 오직 목표로 정한 단 한 곳만 자를 정도로 정확도가 높아졌다는 사실을 발견했다. 0.00000003%의 확률이다. 또 김 단장 팀은 이 기술로 생쥐의 털 색깔을 바꾸는 동물실험에 성공하기도 했다.
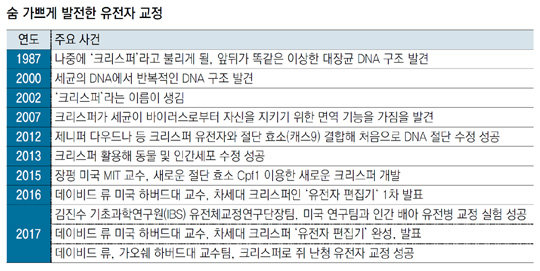
유전자 교정 기술이 어디까지 더 발전할지는 아직 상상하기 힘들다. 올 한 해 이룬 성취가 몹시 크지만, 젊은 기술로서 여전히 앞으로 혁신할 면이 많기 때문이다. 활용 범위도 훨씬 넓어질 것이다. 질병 치료 외에 식량 증산을 위해 작물을 개량하는 데 적용하는 연구도 중국과 유럽 등에서 활발하다.
윤신영 동아사이언스기자 ashilla@donga.com
트렌드뉴스
-
1
목줄 없이 산책하던 반려견 달려들어 50대 사망…견주 실형
-
2
‘면직’ 산림청장, 술 취해 무법질주…보행자 칠뻔, 車 2대 ‘쾅’
-
3
전원주 “벌써 자식들이 재산 노려…인감도장 달래”
-
4
상호관세 대신 ‘글로벌 관세’…韓 대미 투자, 반도체-車 영향은?
-
5
‘신격호 장녀’ 신영자 롯데재단 의장 별세…향년 85세
-
6
“개인회생 신청했습니다” 집주인 통보받은 세입자가 할 일
-
7
연금 개시 가능해지면 年 1만 원은 꼭 인출하세요[은퇴 레시피]
-
8
국토장관 “60억 아파트 50억으로…주택시장, 이성 되찾아”
-
9
국힘 전현직 당협위원장 20여명, ‘절윤 거부’ 장동혁에 사퇴 촉구
-
10
김인호 산림청장 분당서 음주운전 사고…李, 직권면직
-
1
張, 절윤 대신 ‘尹 어게인’ 유튜버와 한배… TK-PK의원도 “충격”
-
2
與 “尹 교도소 담장 못나오게” 내란범 사면금지법 처리 속도전
-
3
국힘 새 당명 ‘미래연대’-‘미래를 여는 공화당’ 압축
-
4
국힘 내부 ‘장동혁 사퇴론’ 부글부글…오세훈 독자 행보 시사도
-
5
김인호 산림청장 분당서 음주운전 사고…李, 직권면직
-
6
[사설]범보수마저 경악하게 한 張… ‘尹 절연’ 아닌 ‘당 절단’ 노리나
-
7
국힘 전현직 당협위원장 20여명, ‘절윤 거부’ 장동혁에 사퇴 촉구
-
8
與 “전두환 2년만에 풀려난 탓에 내란 재발”…사면금지법 강행
-
9
[단독]李 “다주택자 대출 연장도 신규 규제와 같아야 공평”
-
10
목줄 없이 산책하던 반려견 달려들어 50대 사망…견주 실형
트렌드뉴스
-
1
목줄 없이 산책하던 반려견 달려들어 50대 사망…견주 실형
-
2
‘면직’ 산림청장, 술 취해 무법질주…보행자 칠뻔, 車 2대 ‘쾅’
-
3
전원주 “벌써 자식들이 재산 노려…인감도장 달래”
-
4
상호관세 대신 ‘글로벌 관세’…韓 대미 투자, 반도체-車 영향은?
-
5
‘신격호 장녀’ 신영자 롯데재단 의장 별세…향년 85세
-
6
“개인회생 신청했습니다” 집주인 통보받은 세입자가 할 일
-
7
연금 개시 가능해지면 年 1만 원은 꼭 인출하세요[은퇴 레시피]
-
8
국토장관 “60억 아파트 50억으로…주택시장, 이성 되찾아”
-
9
국힘 전현직 당협위원장 20여명, ‘절윤 거부’ 장동혁에 사퇴 촉구
-
10
김인호 산림청장 분당서 음주운전 사고…李, 직권면직
-
1
張, 절윤 대신 ‘尹 어게인’ 유튜버와 한배… TK-PK의원도 “충격”
-
2
與 “尹 교도소 담장 못나오게” 내란범 사면금지법 처리 속도전
-
3
국힘 새 당명 ‘미래연대’-‘미래를 여는 공화당’ 압축
-
4
국힘 내부 ‘장동혁 사퇴론’ 부글부글…오세훈 독자 행보 시사도
-
5
김인호 산림청장 분당서 음주운전 사고…李, 직권면직
-
6
[사설]범보수마저 경악하게 한 張… ‘尹 절연’ 아닌 ‘당 절단’ 노리나
-
7
국힘 전현직 당협위원장 20여명, ‘절윤 거부’ 장동혁에 사퇴 촉구
-
8
與 “전두환 2년만에 풀려난 탓에 내란 재발”…사면금지법 강행
-
9
[단독]李 “다주택자 대출 연장도 신규 규제와 같아야 공평”
-
10
목줄 없이 산책하던 반려견 달려들어 50대 사망…견주 실형
-
- 좋아요
- 0개
-
- 슬퍼요
- 0개
-
- 화나요
- 0개
![합리적 관련성’ 없는 별건 수사 말라는 법원의 경고[오늘과 내일/장택동]‘](https://dimg.donga.com/a/464/260/95/1/wps/NEWS/FEED/Donga_Home_News2/133392680.1.thumb.jpg)


댓글 0