유한양행 3세대 폐암 신약 ‘렉라자’ 1차 치료제 국내 허가
- 동아일보
-
입력 2023년 6월 30일 16시 12분
공유하기
글자크기 설정
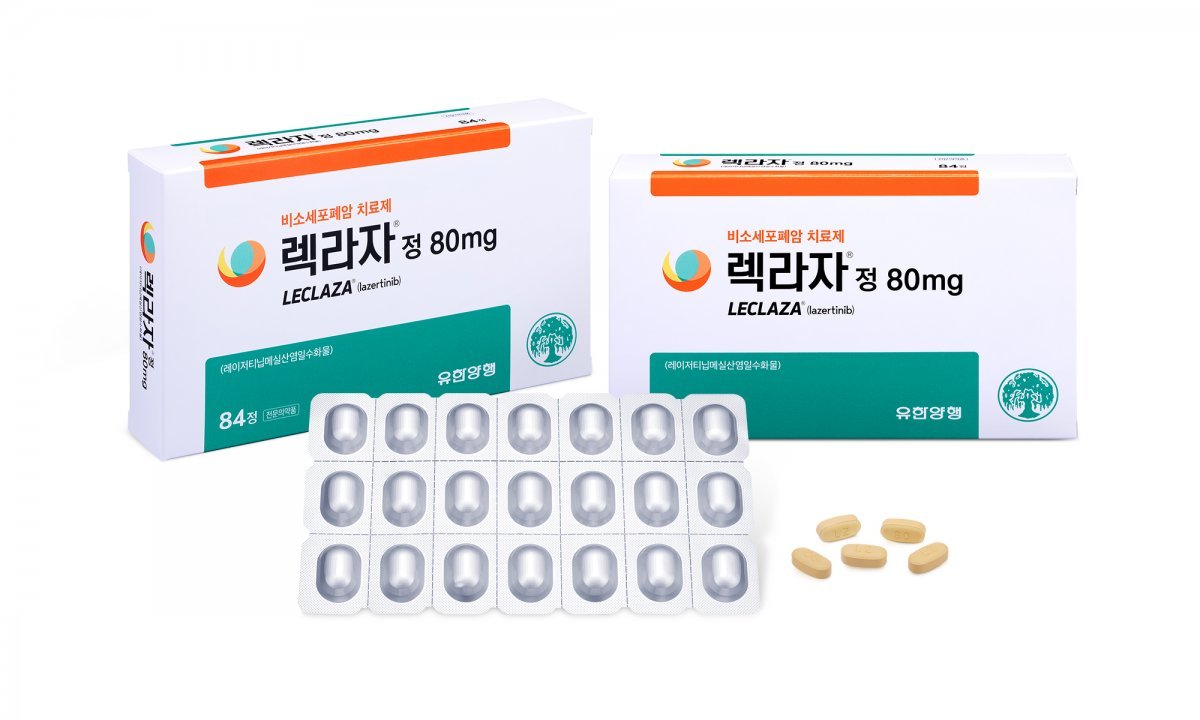
유한양행의 3세대 폐암 신약 ‘렉라자(성분명 레이저티닙)’가 30일 1차 치료제로 식품의약품안전처의 허가를 받았다. 이번 1차 치료제 승인으로 폐암 환자들의 선택의 폭이 넓어질 전망이다.
렉라자는 폐암을 유발하는 여러 돌연변이 중 가장 많은 비중을 차지하는 상피세포 성장인자 수용체(EGFR) 돌연변이 치료에 사용되는 표적 항암제다. 기존의 1, 2세대 EGFR 표적 항암제보다 뇌 전이 환자에게 높은 효과를 보인다. 식약처는 2021년 EGFR 돌연변이 중 EGFR T790M의 양성 2차 치료제로 승인했다.
김열홍 유한양행 R&D 총괄 사장은 “이번 허가로 국내 유병률이 높은 EGFR 변이 양성 비소세포폐암 환자들에게 새로운 치료 옵션을 제공할 수 있게 돼 기쁘다”고 밝혔다.
유한양행은 렉라자의 1차 치료제 급여 기준 확대 신청을 준비하고 있으며, 건강보험 급여 처방 가능 시점까지 환자들에게 무상으로 약제를 제공하는 프로그램(EAP)을 준비하고 있다. 해당 프로그램은 각 기관생명윤리위원회(IRB)의 승인일로부터 렉라자의 급여 기준 확대 시점까지 진행될 예정이다.
유한양행은 2018년 11월에 존슨앤드존슨에 렉라자의 기술수출 및 공동개발 계약을 체결했다. 현재 존슨앤드존슨이 개발한 EGFR-MET 표적의 이중 항체 치료제 ‘아미반타맙’과의 병용 임상을 진행하고 있다.
© dongA.com All rights reserved. 무단 전재, 재배포 및 AI학습 이용 금지
트렌드뉴스
-
1
‘이 질문’에 답변 제대로 못하면 미국 비자 안준다
-
2
주차공간 2개 차지한 포르쉐…“2년째 저주하는 중”
-
3
정용진 부인 콘서트 찾은 트럼프 장남…‘마가 모자’에 사인도
-
4
사우디와 갈라서는 UAE…‘형제국’서 ‘장애물’로 인식 바뀌어
-
5
치매, 50대 후반부터 변화 시작…68~72세 ‘최대 전환시기’ [노화설계]
-
6
72kg 맹견, 6살 소년 20분간 공격…얼굴 뼈 부러져 숨져
-
7
“조응천 출마 제안 처음엔 화내…추미애 나오니 수락”[정치를 부탁해]
-
8
‘무인 공중급유기’ 시험비행 성공…美 “모든 항모에 76대 배치”[청계천 옆 사진관]
-
9
“비둘기 먹으려” 대나무밭서 탕 탕…불법총기로 사냥한 태국인들
-
10
김혜경 여사, 당원병 환아들과 ‘희망쿠키’ 만들기 체험
-
1
정동영 “국힘 숭미주의 지나쳐…‘조선’ 호칭 반대도 그분들 논리”
-
2
반도체 실적 분배 공론화… “사회전체 결실” vs “법인세만 100조”
-
3
국힘 후보들, 장동혁 대신 김문수를 ‘얼굴’로
-
4
10년전 매입-2년 거주 ‘마래푸’, 보유공제 폐지땐 양도세 75% 늘듯
-
5
[사설]‘33년 적자’ 공무원연금, 개혁 더는 못 미룬다
-
6
李 “대외문제서 자해 행위 있어…공적 입장 가져달라”
-
7
北에 ‘조선’ 호칭 논란에… 통일차관 “北실체 인정하는 신뢰의 언어 필요”
-
8
李 ‘소풍 발언’ 역풍에…靑 “교사 본연의 의무 보장하자는 것”
-
9
법무부 “의혹 제기된 검찰 기소, 외부 위원회가 진상 조사”
-
10
한동훈 “李 선거개입” vs 하정우 “제가 통님 설득”…날선 설전
트렌드뉴스
-
1
‘이 질문’에 답변 제대로 못하면 미국 비자 안준다
-
2
주차공간 2개 차지한 포르쉐…“2년째 저주하는 중”
-
3
정용진 부인 콘서트 찾은 트럼프 장남…‘마가 모자’에 사인도
-
4
사우디와 갈라서는 UAE…‘형제국’서 ‘장애물’로 인식 바뀌어
-
5
치매, 50대 후반부터 변화 시작…68~72세 ‘최대 전환시기’ [노화설계]
-
6
72kg 맹견, 6살 소년 20분간 공격…얼굴 뼈 부러져 숨져
-
7
“조응천 출마 제안 처음엔 화내…추미애 나오니 수락”[정치를 부탁해]
-
8
‘무인 공중급유기’ 시험비행 성공…美 “모든 항모에 76대 배치”[청계천 옆 사진관]
-
9
“비둘기 먹으려” 대나무밭서 탕 탕…불법총기로 사냥한 태국인들
-
10
김혜경 여사, 당원병 환아들과 ‘희망쿠키’ 만들기 체험
-
1
정동영 “국힘 숭미주의 지나쳐…‘조선’ 호칭 반대도 그분들 논리”
-
2
반도체 실적 분배 공론화… “사회전체 결실” vs “법인세만 100조”
-
3
국힘 후보들, 장동혁 대신 김문수를 ‘얼굴’로
-
4
10년전 매입-2년 거주 ‘마래푸’, 보유공제 폐지땐 양도세 75% 늘듯
-
5
[사설]‘33년 적자’ 공무원연금, 개혁 더는 못 미룬다
-
6
李 “대외문제서 자해 행위 있어…공적 입장 가져달라”
-
7
北에 ‘조선’ 호칭 논란에… 통일차관 “北실체 인정하는 신뢰의 언어 필요”
-
8
李 ‘소풍 발언’ 역풍에…靑 “교사 본연의 의무 보장하자는 것”
-
9
법무부 “의혹 제기된 검찰 기소, 외부 위원회가 진상 조사”
-
10
한동훈 “李 선거개입” vs 하정우 “제가 통님 설득”…날선 설전
-
- 좋아요
- 0개
-
- 슬퍼요
- 0개
-
- 화나요
- 0개



댓글 0