EMA, 허가 전 개별 국가 조기 사용 검토
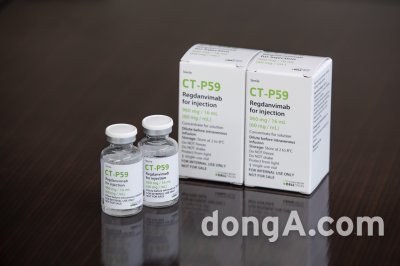
셀트리온, 렉키로나 관련 데이터 EMA 제출 完
글로벌 공급 준비 순항
이번 검토는 지난달 24일부터 진행된 ‘순차 심사(롤링리뷰, Rolling Review)’와 별개로 이뤄지는 절차다. 렉키로나 도입이 시급한 유럽 개별 국가 방역당국이 EMA 품목허가가 나기 전 ‘동정적 사용 프로그램(Compassionate Use Program)’ 등을 통해 도입 결정을 내릴 수 있도록 하기 위한 조치다. EMA 산하 약물사용자문위원회(CHMP) 소속 전문가그룹이 렉키로나 사용 가능 여부에 대한 검증을 진행해 과학적 의견을 제시하는 방식이다.
이번 검토는 코로나19 중등증 환자 및 입원으로 진행될 위험이 높은 고위험군 환자를 대상으로 진행한 셀트리온 임상 데이터를 기반으로 이뤄진다. EMA는 렉키로나가 코로나19 치료제로 중증 발전 비율을 낮추고 집중치료시설 내원 및 입원 비율을 줄일 수 있는지 검증에 들어갈 예정이다.
셀트리온 관계자는 “글로벌 신속 승인 절차 완료 후 즉시 원활한 공급을 위해 물량 확보를 차질 없이 진행하고 있다”며 “10만 명분 생산을 완료했고 즉각적인 공급에 대응할 수 있도록 수요에 따라 연간 150만~300만 명분 렉키로나를 추가로 생산할 계획”이라고 말했다.
동아닷컴 김민범 기자 mbkim@donga.com
-
- 좋아요
- 0개
-
- 슬퍼요
- 0개
-
- 화나요
- 0개
-
- 추천해요
- 개
지금 뜨는 뉴스
-
![“파마·커트가 80만 원, 이거 사기인가요”…한국 온 일본인 당황 [e글e글]](https://dimg.donga.com/a/464/260/95/1/wps/NEWS/FEED/Donga_Home_News/124557349.2.thumb.jpg)
“파마·커트가 80만 원, 이거 사기인가요”…한국 온 일본인 당황 [e글e글]
- 좋아요 개
- 코멘트 개
-
![[이기홍 칼럼]김건희 여사 엄정한 사법처리만이 尹정권 살길이다](https://dimg.donga.com/a/464/260/95/1/wps/NEWS/FEED/Donga_Home_News/124552515.1.thumb.jpg)
[이기홍 칼럼]김건희 여사 엄정한 사법처리만이 尹정권 살길이다
- 좋아요 개
- 코멘트 개
-

5호선 하남 검단산행 발산역 운행 ‘8분 지연’…“현재 정상 운행”
- 좋아요 개
- 코멘트 개
댓글 0